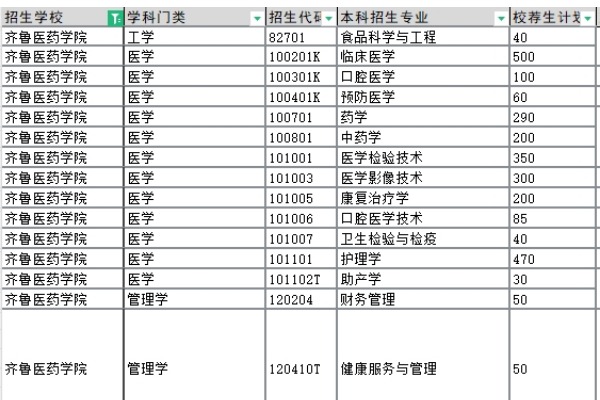
近日齐鲁医药学院发布2023年普通高等教育专科升本科专业综合测试考试大纲,以下为《分析化学》科目考试大纲,备考生一起来看看吧~
一、考试题型和分值
(一) 考试题型:单项选择题、多项选择题
(二) 总分:100 分
二、参考教材
《分析化学》,化学工业出版社,第二版,主编 王文渊 黄锁义 邢占芬
三、考试范围
第一章 绪论
1.分析化学的分类。结构分析、定性分析与定量分析;无机分析与有机 分析;常量、半微量、微量与超微量分析;例行分析与仲栽分析。
2.分析化学的任务和作用以及发展和趋势,尤其是在国民经济、科学研 究、医药卫生、学校教育等方面的重要作用。
第二章 误差与分析数据处理
1.误差的产生与分类;绝对误差、相对误差、理论真值、约定真值、相 对真值、标准参考物质、系统误差与偶然误差、准确度、精密度等基本概念。 绝对误差和相对误差的区别和计算方法、系统误差和偶然误差区别以及判断 方法、准确度与精密度的关系、准确度与误差的关系、精密度与偏差的关系
2.测量误差:掌握偏差、相对平均偏差、标准偏差、相对标准偏差的基 本概念以及计算公式。熟悉提高分析准确度的方法
3.有效数字的基本概念以及作用;灵活应用有效数字运算法则和数字修 约规则。
第三章 滴定分析法概述
1.化学计量点、滴定、容量分析法的基本概念和适用于滴定分析的化学 反应具备的三个条件;滴定分析的种类、滴定分析的方式。
2.符合基准物质的条件、标准溶液浓度的表示方法;灵活应用直接法和 间接法配制标准溶液;常见的基准物质的组成、干燥的温度、标定对象。
3.滴定分析的依据,熟练应用滴定分析的计算。
第四章 酸碱滴定法
1.质子论酸碱的定义、酸碱反应的实质、溶剂的质子自递反应和质子自 递常数的概念、衡量酸碱强度的规律。
2.酸的浓度和酸度的关系、酸碱分布系数的概念、酸度对酸碱型分布的 影响;掌握酸碱分布系数计算公式、特点、计算方法。
3.酸碱溶液的质子条件和一元酸碱、多元酸碱、两性物质、缓冲溶液计 算公式的推导;记住一元酸碱、多元酸碱、两性物质、缓冲溶液计算公式; 灵活应用一元酸碱、多元酸碱、两性物质、缓冲溶液计算公式。
4.指示剂的变色原理、指示剂的变色范围,了解影响指示剂变色范围的
因素,并可根据类型不同的酸碱反应灵活选择指示剂。 5.酸碱滴定曲线的绘制,掌握影响酸碱滴定突跃的因素、进行酸碱准确
滴定的条件。了解滴定终点误差的基本概念和计算公式,掌握酸碱滴定终点 误差的计算。
6.常见酸、碱溶液的配制和标定,直接酸碱滴定和间接酸碱滴定的原理。 7.质子溶剂、非质子溶剂、混合溶剂等概念。 8.溶剂的解离性、溶剂的酸碱性、溶剂的极性、区分效应和均化效应。
第五章 沉淀滴定法
1.沉淀滴定法的基本概念以及符合沉淀滴定法的基本条件。 2.银量法的基本原理,滴定曲线的绘制、影响滴定突跃的因素; 3.指示终点的方法(铬酸钾指示剂法、铁铵矾指示剂法、吸附指示剂法)。 4.标准溶液的配制与标定和常用的指示剂。 5.无机卤代物、有机氢卤酸盐和有机卤化物的测定和计算方法。
第六章 配位滴定法
1.介绍配位滴定法作用、条件;氨羧配位剂和 EDTA 配位剂的特点。
2.配位滴定法的基本原理:讲解稳定常数、累积稳定常数、副反应系数、 条件稳定常数的基本概念、计算和作用;配位反应中的副反应(酸效应和配位 效应)金属指示剂的作用原理、金属指示剂颜色转变点 PMt 的计算和常用的 金属指示剂;详细讲解滴定终点误差的计算。
3.配位滴定法滴定条件的选择;酸度如何选择,最高酸度、最低酸度、 最佳酸度的确定;掩蔽剂选择方法以及配位掩蔽剂的用量。
4.EDTA 标准溶液和常用的指示剂 (铬黑 T、二甲酚橙) 的配制、标准溶 液的标定。
5.滴定方法与示例:理解直接滴定法、返滴定法、间接滴定法、置换滴 定法的概念和实质。
第七章 氧化还原滴定法
1.氧化还原滴定法的一些基本概念和分类、适用于氧化还原滴定的条件。
2.引入条件电位的原因、概念、作用;影响条件电位的因素 (盐效应、 生成沉淀、生成配合物、酸效应) ;介绍氧化还原反应进行的程度,氧化还 原反应的速度。
3.氧化还原指示剂的变色原理;常见氧化还原指示剂的特点。
4.碘量法的基本原理:掌握碘的标准溶液、硫代硫酸钠标准溶液的配制 和标定,掌握直接碘量法、剩余碘量法、置换碘量法的运用。
5.高锰酸钾法的基本原理;高锰酸钾溶液的配制和标定,高锰酸钾法优 缺点。
6.亚硝酸钠法的基本原理和应用。
研究考试大纲,对大纲中的考点及相关要求进行认真研究,是应考的关键。正在备考专升本的同学,关注山东好老师升学帮网站可以了解更多专升本的考试信息。如果在学习上有困难,自制力差,可以在下方留下你的联系方式,我们的老师会针对你的学习情况给出建议。
 抖音
抖音

 微信
微信

 微博
微博

 QQ群
QQ群

 400-023-1785
400-023-1785